
SUUR LUGU! Dokumendid: EMA-d survestati kiirustama Pfizeri vaktsiini heakskiiduga ohutuse arvelt
Artikli kuulamine on saadaval MINU TELEGRAM tellijatele
21. juuli 2022 kell 12:30

Foto: bizoo_n / Adobe Stock + ekraanikuvad + Canva.com
Euroopa Ravimiameti (EMA) lekkinud dokumentide kohaselt avaldasid Ameerika Ühendriikide ja Euroopa Liidu valitsusametnikud Euroopa ravimiregulaatorile survet, et nad kiirustaksid Pfizeri/BioNTechi COVID-19 mRNA vaktsiini (eksperimentaalse geeniteraapia) heakskiitmist ohutusprobleemidest hoolimata.
Artikli autoriks on PhD Michael Nevradakis, sõltumatu Kreeka ajakirjanik ja teadlane.
Dokumendid hõlmavad e-kirju, PowerPointi esitlust ja konfidentsiaalset Pfizeri aruannet 10.–25. novembrini 2020 – vaid nädalaid enne seda, kui Euroopa, Ühendkuningriigi ja USA regulaatorid andsid loa “vaktsiini” hädaolukorras kasutamiseks.
Peamiselt selgub dokumentidest:
- “Vaktsiini” kiire heakskiitmine, mida kiirustasid tagant USA ja Euroopa valitsustegelased.
- Surve Euroopa reguleerivatele asutustele Pfizeri “vaktsiini” heakskiitmiseks, hoolimata ekspertide murest “vaktsiini” ohutuse pärast.
- Olulised erinevused mRNA efektiivsuses “vaktsiini” proovipartiide ja Pfizeri/BioNTechi COVID-19 viaalide kaubanduslike partiide vahel, mis tõstatab ohutusprobleeme.
- FDA ei tunne nende erinevuste vastu suurt huvi.
- mRNA-ga seotud vastuvõetava läve langetamine vahetult enne seda, kui Pfizeri/BioNTechi eksperimentaalne geeniravi sai Ühendkuningriigis, USA-s ja ELis regulatiivse heakskiidu.
- Pfizeri tegevjuhi Albert Bourla otsene lobitöö, mis suunatud Euroopa Komisjoni presidendile ja kõrgetasemelisele FDA regulaatorile.
Poliitikud pingutasid kõvasti, et Pfizeri geeniteraapia heakskiitmisega kiirustada
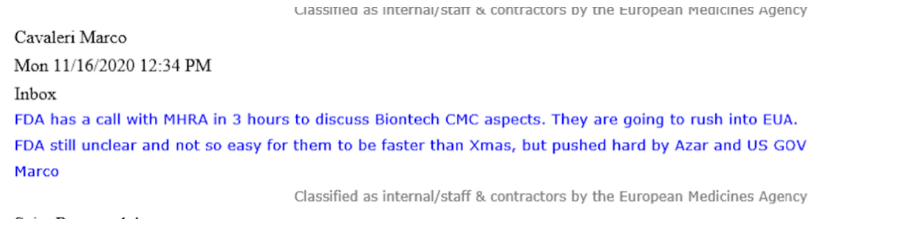
16. novembril 2020 saadetud e-kirjas väitis Marco Cavaleri, tollane EMA bioloogiliste terviseohtude ja vaktsiinide strateegia juht, et “[Alex] Azar ja USA valitsus” olid “kõvasti surunud”, et “saada kiirustades vaktsiinidele hädaolukorra kasutusluba (EUA). Azar oli sel ajal USA tervishoiu- ja sotsiaalteenuste minister, ministeeriumi haldusalas on ka FDA (mis on EMA USA vaste – toim.).
19. novembril 2020 saadetud e-kirjas viitas EMA tollane tegevdirektori asetäitja Noel Wathion – telekonverentsi stenogrammile – “volinikuga”, pidades silmas Euroopa Komisjoni volinikku Ursula von der Leyenit.
Kõne ajal, mida Wathion kirjeldas kui “üsna pingelist, kohati isegi veidi ebameeldivat”, hoiatas von der Leyen EMA-d, mis võib juhtuda, “kui ootused ei täitu”, et kiiresti väljastada CMA [Euroopa Liidu tingimuslik müügiluba].
Samas elektronkirjas kirjutas Wathion:
“Poliitiline väljalangevus näib olevat liiga suur, isegi kui “tehniline tase” … suudaks sellist viivitust kaitsta, et muuta teadusliku ülevaate tulemused võimalikult tugevaks.” …
“Kuigi me teame, et mida iganes me teeme (protsessi kiirendamine, et viia võimalikult palju vastavusse FDA/MHRA (ravimite ja tervishoiutoodete reguleeriva ameti) nn heakskiitmise ajastusega versus ajakulu, mis on vajalik kindluse saamiseks eelkõige seoses CMC [keemia-, tootmis- ja kontrollijuhised] ja ohutusega), seisab EMA mitmenädalase hilinemise korral silmitsi väljakutsega vastata erinevate osapoolte küsimustele ja kriitikale.”
Wathioni viidatud “erinevad osapooled” hõlmasid Euroopa Komisjoni, Euroopa Parlamenti, meediat ja avalikkust.
Wathion väitis, et “CMC vastutus ja usaldusväärsus on minu arvates kindlasti elemendid, mida tuleb arvesse võtta.”
Hilisemas e-kirjas, 22. novembril 2020, paljastas Wathion, millega agentuur Pfizeri/BioNTechi geenisüstidele tingimusliku müügiloa väljastamiseks silmitsi seisis, kirjutades:
“Tõenäosus, et FDA (ja ka MHRA) väljastab EUA (hädaolukorra kasutusloa) enne CMA (EL tingimuslik müügiluba) andmist on äärmiselt suur. Seega peame selleks valmistuma.”
Wathion väljendas samas e-kirjas muret, et selline ettevalmistus võib toimuda
Palun oota...
Tegemist on tasulise artikliga, edasi lugemiseks palun logi sisse või hakka liikmeks.
1 kuu
10.88€
(130.56€ 1 aasta)6 kuud
50€
(8.33€ 1 kuu)1 aasta
88€
(7.33€ 1 kuu)Kuldpakett 1 aasta
188€
(58€ aasta / 4.83€ kuu +*) + 1g kuldplaat väärtus 130€, limiteeritud kogus!
Võimalik tasuda kolmes osas













Kommentaarid
Kommentaare lugeda ja kommenteerida saavad vaid Minu Telegrami tellinud kasutajad. Tellimuse esitamiseks kliki siia või logi sisse siit.